Unterschied zwischen physikalischen und chemischen Eigenschaften
- 3011
- 36
- Leonhard Lesch

Was sind physikalische Eigenschaften?
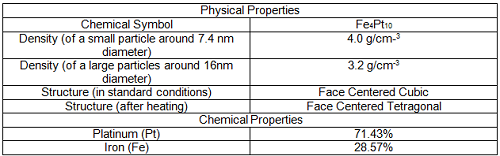
Physikalische Eigenschaften sind solche, die beobachtet und gemessen werden können, ohne die tatsächliche Zusammensetzung der Materie zu ändern. Die chemische und molekulare Zusammensetzung bleibt unabhängig von der verwendeten Messmethode gleich.
Jede Eigenschaft, die ohne chemische Reaktion nachgewiesen und gemessen werden kann, ist somit eine physikalische Eigenschaft.
Physikalische Veränderungen können auftreten, e.G. Änderung der Zustände, aber dies verändert nur die physikalische Form nicht die chemische Struktur oder molekulare Zusammensetzung der Substanz. Zum Beispiel ändert sich beim Einfrieren des Wassers die chemische Natur des Wassers nicht, sodass ein Gefrierpunkt eine weitere physikalische Eigenschaft ist.
Materiezustände sind auch eine physikalische Eigenschaft, da alle Substanzen in einer festen, flüssigen oder gasischen Phase in Abhängigkeit von Energieverlust oder Gewinn existieren können.
Das gleiche Element ist nach der Änderung und im gesamten Prozess vorhanden. Körperliche Veränderungen hängen mit physischen Eigenschaften zusammen.
Physikalische Eigenschaften können umfangreich oder intensiv sein:
- Umfangreiche Abhängigkeiten von der gemessenen Materie, zum Beispiel, Masse, Volumen und Länge.
Umfangreiche Eigenschaften sind extern, das ist, dass die Substanz nicht mit diesen identifiziert werden kann, und der Wert ändert sich je nach Betrag der vorhandenen Substanz. Zum Beispiel können Sie 10 g Öl oder 10 g Wasser messen. Dies ermöglicht Ihnen jedoch nicht, eine Substanz als Öl oder Wasser zu identifizieren.
- Intensiv - hängen nicht von der Menge an Materie ab, z. B. Farbe, Dichte, Viskosität, Auftrieb, Schmelzpunkt, Gefrierpunkt.
Intensive Eigenschaften sind immer gleich und können verwendet werden, um zu ermitteln, was eine Substanz ist. E.G. Dichte des flüssigen Wassers beträgt 1 g/ml, der Siedepunkt 100 beträgt 100ÖC und der Gefrierpunkt sind 0ÖC.
Durch die Verwendung mehrerer intensiver Eigenschaften zusammen kann man eine Substanz identifizieren. Substanzen können auch basierend auf ihren physikalischen Eigenschaften klassifiziert und gruppiert werden.
Beispiele für physikalische Eigenschaften sind:
- Temperatur
- Formbarkeit
- Aussehen
- Textur
- Farbe
- Geruch
- Form
- Löslichkeit
- Elektrische Ladung
- Molekulargewicht
- Siedepunkt
- Schmelzpunkt
- Gefrierpunkt
- Volumen
- Masse
- Länge
- Dichte
- Löslichkeit
- Polarität
- Viskosität
- Druck
- Elektrische Ladung
- Härte
Was sind chemische Eigenschaften?
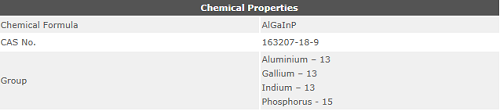
Eine chemische Eigenschaft bedeutet per Definition, dass die Messung der Eigenschaft zu einer Änderung der tatsächlichen chemischen Struktur der Substanz führt. Chemische Eigenschaften werden deutlich, wenn die Substanz eine chemische Veränderung oder Reaktion erfährt.
Chemische Eigenschaften beschreiben die Fähigkeit einer Substanz, sich mit anderen Substanzen zu verbinden oder sich in ein anderes Produkt zu verwandeln. Es ist eine Möglichkeit zu beschreiben, mit welchem Substanz reagieren könnte oder sich am Ende ändern könnte. Wenn eine chemische Reaktion auftritt, ändert sich Materie zu einer völlig anderen Art von Materie.
Zum Beispiel kann Natrium mit Wasserdampf in der Luft reagieren und heftig explodieren. Eisen und Sauerstoff kombinieren zu Rost, so dass Eisen die chemische Fähigkeit hat, Rost zu bilden. Benzin hat die Fähigkeit zu brennen (es ist brennbar).
Eine chemische Eigenschaft ist jede Qualität, die nur festgelegt werden kann, wenn eine Änderung in der chemischen Identität der Substanz vorgenommen wird. Einfaches Berühren oder Beobachten einer Substanz zeigt ihre chemischen Eigenschaften nicht. Die Struktur der Materie oder Substanz muss geändert werden, um die chemische Eigenschaft zu sehen.
Chemische Eigenschaften sind nützlich zu wissen, da dies bei der Identifizierung unbekannter Substanzen oder beim Versuch, Substanzen zu trennen oder zu reinigen, hilft und Wissenschaftlern ermöglichen, Substanzen wie Verbindungen zu klassifizieren.
Wenn Wissenschaftler diese Eigenschaften kennen, können Wissenschaftler Anwendungen entwickeln, bei denen verschiedene Substanzen verwendet werden können.
Wissenschaftler können auch vorhersagen, wie Proben in einer chemischen Reaktion reagieren, wenn sie die chemischen Eigenschaften der Substanzen vorhanden haben.
Einige Beispiele für chemische Eigenschaften umfassen Folgendes:
- Toxizität
- Chemische Stabilität (wenn eine Verbindung mit Wasser oder Luft reagiert)
- Verbrennungswärme
- Entflammbarkeit (ob die Verbindung brennt, wenn sie Flamme ausgesetzt ist)
- Reaktivität (Fähigkeit, mit anderen Chemikalien zu reagieren)
- Enthalpie der Formation
- Oxidationszustände (Sauerstoff gewinnen, Wasserstoff verlieren oder Elektronen verlieren und dazu führen, dass die Oxidationszahl einer Substanz geändert wird. Ein Beispiel hierfür wäre Rost).
- Arten von chemischen Bindungen, die sich bilden (ob kovalent, nicht kovalent oder Wasserstoff)
- Auftrieb
- Viskosität
- Kompressibilität
- Radioaktivität (Strahlungsemission aus einem Atom)
- Halbwertszeit
Was ist der Unterschied zwischen physikalischen und chemischen Eigenschaften?
- Physikalische Eigenschaften sind jene Eigenschaften, die ohne beobachtet oder gemessen werden können
Eine Änderung der Materie verursacht oder führt, während chemische Eigenschaften erst beobachtet werden, nachdem sich eine Änderung der Angelegenheit verändert hat.
- Physikalische Eigenschaften können Zustände verändern, ohne die molekulare Struktur zu ändern, aber dies ist bei chemischen Eigenschaften nicht der Fall.
- Bei chemischen Eigenschaften wird die chemische Identität der Substanz geändert, dies ist bei den physikalischen Eigenschaften nicht der Fall.
- Bei chemischen Eigenschaften ändert sich die Struktur des Materials, während sich die Struktur bei physikalischen Eigenschaften nicht ändert.
- Eine chemische Reaktion tritt auf, bevor eine chemische Eigenschaft offensichtlich wird, während keine chemische Reaktion erforderlich ist, damit eine physikalische Eigenschaft sichtbar wird.
- Chemische Eigenschaften können im Gegensatz zu physikalischen Eigenschaften verwendet werden, um vorherzusagen, wie Substanzen reagieren.
Tabelle Vergleich der physikalischen und chemischen Eigenschaften
| Physikalische Eigenschaft | Chemische Eigenschaft |
| Beobachtet, ohne eine Veränderung herbeizuführen | Erst beobachtet, nachdem er eine Veränderung herbeigeführt hat |
| Kann den physischen Zustand verändern, aber keine Moleküle | Verändert immer Moleküle |
| Chemische Identität bleibt gleich | Chemische Identitätsänderungen |
| Die Struktur des Materials ändert sich nicht | Struktur von Materialänderungen |
| Es ist keine chemische Reaktion erforderlich, um die Eigenschaft zu zeigen | Es ist eine chemische Reaktion erforderlich, um Eigenschaften zu zeigen |
| Kann nicht verwendet werden, um vorherzusagen, wie Substanzen reagieren werden | Kann verwendet werden, um vorherzusagen, wie Substanzen reagieren werden |
Zusammenfassung:
- Physikalische Eigenschaften können beobachtet werden, ohne dass sich eine Änderung in dieser Angelegenheit unterziehen muss.
- Physikalische Eigenschaften können je nach Materie variieren, z. B. Länge, Volumen und Masse. Diese sind als umfangreiche physikalische Eigenschaften bekannt.
- Intensive physikalische Eigenschaften hängen nicht von der Menge an Materie ab, e.G. Textur.
- Physikalische Eigenschaften können die Zustände ändern, aber dennoch die gleiche chemische Struktur behalten, e.G. Einfrieren oder Kochen von Wasser.
- Chemische Eigenschaften können nur mit einer Änderung beobachtet werden, wie z. B. eine chemische Reaktion.
- Materie wird beide basierend auf ihren physikalischen und chemischen Eigenschaften klassifiziert.
- « Unterschied zwischen funkelndem Wasser und Soda -Wasser
- Unterschied zwischen einem verwalteten und nicht verwalteten Schalter »

