Differenz zwischen Bioburden und mikrobieller Grenze -Test
- 4826
- 1517
- Kurt Reinelt
Das Gebiet der pharmazeutischen Mikrobiologie hat sich im Laufe der Jahre aufgrund der jüngsten technologischen Fortschritte entwickelt, begleitet von der Veröffentlichung neuer und harmonisierter Kompendienmethoden. Aus diesem Grund ist es für Mikrobiologen, die für die Überwachung der mikrobiellen Qualität der pharmazeutischen Produkte verantwortlich sind, unerlässlich, um mit den Änderungen Schritt zu halten. Die mikrobiologische Qualität der fertigen Produkte wird durch die Qualität der Ausgangsmaterialien bestimmt, die in den meisten Fällen nicht sterile Materialien oder Produkte sind. Solche Produkte werden entweder verwendet, um komplexere pharmazeutische Produkte herzustellen oder in den vorläufigen Stadien der sterilen Produkte zu werden.
Obwohl die meisten der veröffentlichten Produkte keine Sterilisation erfordern, werden einige Produkte auf das Vorhandensein von anstößigen Mikroorganismen getestet. Das Vorhandensein bestimmter Mikroorganismen in einigen nichtsterilen Produkten kann die therapeutischen Eigenschaften des Produkts und in einigen Fällen die Gesundheit des Patienten beeinflussen. Für diese Produkte sind also zusätzliche Tests für Indikator -Mikroorganismen erforderlich. Die mikrobielle Untersuchung oder das Testen dieser nichtsterilen Produkte wird durch „mikrobieller Grenzwerte-Test“ durchgeführt, der die Bioburden des Produkts bestimmt. Bioburden bezieht sich auf die Anzahl der Mikroorganismen auf einer Oberfläche oder in einer Lösung, die nicht sterilisiert wurde.

Was ist A Bioburden -Test?
Bioburden bezieht sich auf die Anzahl der Mikroorganismen, die auf einem Gegenstand oder einer Oberfläche oder in einer Lösung nachgewiesen werden können. Es ist notwendig, die anfängliche Anzahl von Mikroorganismen für die Auswahl von Parametern für jede Methode zum Abtöten von Mikroorganismen zu kennen. Diese anfängliche Zahl wird als "Bioburden" oder "Bioload" bezeichnet. Die verwendete mikrobielle Wiederherstellungsmethode hängt von der Art des zu bewertenden Materials ab. Die Notwendigkeit einer gründlichen Analyse von Bioburden ist ein Bereich, der im Validierungsprozess häufig unterschätzt wird. Ein Bioburden -Test wird für Qualitätskontrollzwecke durchgeführt, um die mikrobiellen Kontaminationsniveaus auf oder in einem Produkt zu messen. Es handelt sich um einen TEG -Test (Total Lentable Count), um die tragfähigen aeroben mesophilen Mikroorganismen in Produkten oder Artikeln abzuschätzen, die nicht steril sind. Kenntnis des Bioburden.
Was ist ein mikrobieller Grenzwerttest?
Der mikrobielle Grenzwerttest ist der "Test für bestimmte Mikroorganismen" zur Bestimmung der qualitativen und quantitativen Abschätzung von lebensfähigen aeroben Mikroorganismen in pharmazeutischen Produkten natürlicher oder biologischer Herkunft, Rohstoffe und fertigen Produkte. Rohstoffe sind Produkte, die zur weiteren Verarbeitung oder zur Unterstützung einer solchen Verarbeitung verwendet werden können. Nicht sterile Produkte werden auf lebensfähige Mikroorganismen zur Nachweis von Krankheitserregern und Gesamtzahlen getestet. Die mikrobiologische Qualität von nicht-pharmazeutischen oder kosmetischen Produkten kann unter Verwendung der Schätzung der gesamten lebensfähigen Anzahl und der Erkennung des Vorhandenseins spezifischer mikrobieller Spezies in diesen Substanzen kontrolliert werden. Der mikrobielle Grenze -Test umfasst die gesamte aerobe mikrobielle Anzahl (TAMC), die Gesamthefe und Schimmelpilze (TYMC) und Tests auf Indikatororganismen. Das Ziel des mikrobiellen Grenzwerttests ist ziemlich einfach - Mikroorganismen auszuschließen, die anschließend zu einer Verschlechterung des Produkts führen oder dem Patienten schaden können.
Differenz zwischen Bioburden und mikrobieller Grenze -Test
Prüfen
- Der mikrobielle Grenzwerttest bestimmt den Bioburden bestimmter pharmazeutischer Herstellungsproben für Qualitätskontrollzwecke. Bioburden bezieht sich auf die Anzahl der Mikroorganismen auf einer Oberfläche oder in einer Lösung, die nicht sterilisiert wurde. Der Bioburden -Test wird durchgeführt, um die mikrobiellen Kontaminationsniveaus auf oder in einem Produkt zu bewerten. Kenntnis des Bioburden. Der mikrobielle Grenzwert wird die Informationen zur Durchführung von Bioburden -Zahlen durch quantitative Schätzung lebensfähiger aeroben Mikroorganismen in pharmazeutischen Artikeln, Rohstoffen und fertigen Produkten liefern. Der Bioburden -Test wird auch als Gesamtzahl bezeichnet.
Methode
- Der Bioburden -Test bestimmt die Anzahl der Mikroorganismen auf einem Gegenstand oder einer Oberfläche oder in einer Lösung. Ein Nachhaltigkeitstest muss zuerst vor dem tatsächlichen Bioburden -Test durchgeführt werden, um sicherzustellen. Der Bioburden -Test ist entweder eines oder beide der kompendialen TAMC -Methoden (Total Aerobic Microbials Count) oder TYMC (Total Hefe- und Schimmelpilzzahl) oder eine Alternative. Für die mikrobielle Beurteilung und Untersuchung gibt es vier empfohlene Methoden: Membranfiltration, direkte Beplattierung, Spreadplatte und serielle Verdünnung.
Zielsetzung
- Das Ziel des Bioburden -Tests besteht darin, die Gesamtzahl der auf medizinischen Geräte vorhandenen medizinischen Mikroorganismen vor ihrer endgültigen Sterilisation zu messen und dann die Nummer zu verwenden, um die am besten geeigneten Parameter für ihre endgültige Sterilisation zu bestimmen, bevor sie verwendet werden. Nicht sterile Produkte werden auf lebensfähige Mikroorganismen zur Nachweis von Krankheitserregern und Gesamtzahlen getestet. Der mikrobielle Grenzwert (MLT) wird durchgeführt, um die qualitative und quantitative Schätzung tragfähiger aeroben Mikroorganismen in nicht sterilen pharmazeutischen Herstellungsproben zu bewerten, die von Rohstoffen bis hin zu fertigen Produkten reichen.
Bioburden vs. Mikrobieller Grenzwerttest: Vergleichstabelle
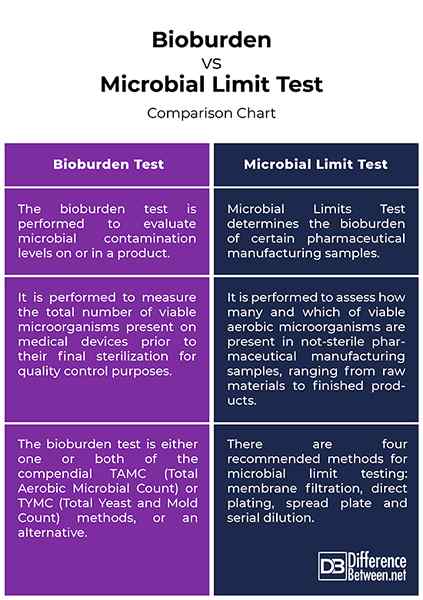
Zusammenfassung
Kurz gesagt, nicht sterile Produkte werden auf praktikable Mikroorganismen zur Nachweis von Krankheitserregern und Gesamtzahlen getestet. Während die meisten der veröffentlichten Produkte keine Sterilisation erfordern, werden einige Produkte auf das Vorhandensein von anstößigen Mikroorganismen getestet. Das Vorhandensein bestimmter Mikroorganismen in bestimmten nichtsterilen Produkten kann die therapeutischen Eigenschaften des Produkts beeinflussen. Die mikrobielle Untersuchung oder das Testen dieser nichtsterilen Produkte wird durch „mikrobieller Grenzwerte-Test“ durchgeführt, der das Produktbioburden bestimmt, das sowohl Rohstoffe als auch Fertigprodukte umfasst.
- « Unterschied zwischen Bronchitis und Pleuritis
- Unterschied zwischen Fettleibigkeit und Depression im Kindesalter »

