Unterschied zwischen ionischer und kovalenter Bindung
- 3322
- 505
- Hr. Jeremie Orth
 Ionische gegen kovalente Bindung
Ionische gegen kovalente Bindung
In der Chemie wird ein Molekül und eine Verbindung gebildet, wenn zwei oder mehr Atome über einen chemischen Prozess, der als Bindung bezeichnet wird. Es gibt zwei Arten der chemischen Bindung „kovalent und ionisch. In der ionischen Form der chemischen Bindung tun die Atome, die miteinander verbunden sind. Bei der chemischen Bindung haben die Atome jedoch Elektronen.
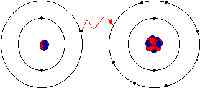
In der ionischen Bindung werden die Elektronen vollständig von einem der Bindungsatome auf den anderen übertragen. Es sind die elektrostatischen Kräfte, die die Ionen mit der entgegengesetzten Ladung machen, um sich voneinander anzusehen. Zum Beispiel verliert Natrium in einer ionischen Bindung zwischen Natrium und Chlor sein einziges Elektron, das dem negativ geladenen Chlorion positiv geladen wird. Bei der Ionenbindung schrumpft das Atom, das seine Elektronen verliert, und das Atom -Gewinn -Elektronen wächst in der Größe. Dies ist nicht so bei der kovalenten Bindung, in der Ionen gleichermaßen geteilt werden. Kovalente Bindung findet statt, wenn die Atome auftreten, weil die Atome in der Verbindung eine ähnliche Fähigkeit haben, Ionen zu gewinnen und zu verlieren. Daher können sich Ionenbindungen zwischen Metallen und Nichtmetallen bilden, während sich zwischen zwei Nichtmetallen kovalente Bindungen bilden.
 Ionenbindungen können auch in Wasser und anderen Arten von polaren Lösungsmitteln gelöst werden. Auch ionische Verbindungen sind sehr gute Elektrizitätsleiter. Ionenbindungen führen auch zur Bildung kristalliner Feststoffe mit einer hohen Schmelztemperatur. Ionische Verbindungen sind auch immer Feststoffe.
Ionenbindungen können auch in Wasser und anderen Arten von polaren Lösungsmitteln gelöst werden. Auch ionische Verbindungen sind sehr gute Elektrizitätsleiter. Ionenbindungen führen auch zur Bildung kristalliner Feststoffe mit einer hohen Schmelztemperatur. Ionische Verbindungen sind auch immer Feststoffe.
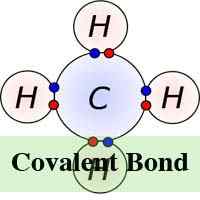
Im Gegensatz zur ionischen Bindung erfordert die kovalente Bindung, dass Moleküle in ihrer wahren Form existieren, und daher werden kovalente Moleküle nicht voneinander angezogen, sondern in Flüssigkeiten oder Gasen bei Raumtemperatur frei existieren. Die kovalente Bindung kann auch zu einer Mehrfachverbindung führen, die im Gegensatz zu einer ionischen Bindung. Dies liegt daran, dass einige Atome in der Lage sind, mehrere Elektronenpaare zu teilen, wodurch gleichzeitig mehrere kovalente Bindungen gebildet werden.

