Unterschied zwischen Brom und Chlor

- 4523
- 308
- Justus Dengler
Die Gruppe des Periodensystems umfasst die Elemente Fluor (F), Chlor (CL), Brom (BR), Jod (I) und Astatine (AT). Alle diese Elemente sind unter dem generischen Namen „Halogenelemente“ bekannt und haben nichtmetallische chemische Eigenschaften.

Was ist Brom??
- Brom (BR) ist ein nichtmetales chemisches Element der VIIA-Gruppe des periodischen Systems, das unter normalen Bedingungen eine rotbraune Flüssigkeit mit einem hoch irritierenden Geruch ist.
- Brom ist die Nummer 35 in der Periodenzüchter und hat eine Atommasse von 79.904.
- Es ist weniger reaktiv als Chlor. Unter normalen Bedingungen nimmt Brom jedoch an mehreren chemischen Wechselwirkungen teil.
- Eine wässrige Lösung von molekularem Brom (2.8%) wird als Bromwasser bezeichnet und in vielen organischen Reaktionen verwendet. Im Allgemeinen ist das Brom in organischen Lösungsmitteln sehr gut löslich. Oft zeigt es in den Verbindungen einen Oxidationszustand von -1, kann aber auch in jedem seltsamen positiven Oxidationszustand sein (+1, +3, +5, +7).
- In der Natur tritt Brom in Form einer Mischung aus zwei stabilen Isotopen auf. Es ist als Unreinheit in den Chlormineralien Halit (NaCl - Salz), Sylvite (KCL), Carnallit (Kaliummagnium -Hexahydrat) usw. enthalten. Der Gehalt im Meerwasser beträgt ungefähr 1: 660 Chloratome.
- Die Verwendung von Brom umfasst pharmazeutische Präparate, Pestizide, Farbstoffe, Flammschutzmittel usw. In der Vergangenheit wurde Kaliumbromid als Beruhigungsmittel und Antikonvulsiva verwendet.

Was ist Chlor?
- Chlor (CL) ist ein nichtmetales chemisches Element der VIIA-Gruppe des periodischen Systems, das unter normalen Bedingungen in Form eines grünlich-gelben Gases mit einem hoch irritierenden Geruch ist.
- Chlor ist die Nummer 17 in der Periodenzüchter und hat eine Atommasse von 35.453.
- Chlor ist ein extrem aktives chemisches Element. Bei chemischen Wechselwirkungen scheint es normalerweise ein starkes Oxidationsmittel zu sein, und in seinen chemischen Verbindungen ist es am häufigsten von -1 Oxidationszustand. Wenn es im Molekül ein stärkeres Oxidationsmittel gibt, weisen die Chloratome einen positiven Oxidationszustand auf. Zum Beispiel in der Perchlorsäure erreicht der Oxidationszustand der Chloratome +7. Chlor kann in allen Oxidationszuständen von -1 bis +7 vorhanden sein, außer +2.
- In Natur. Die Mineralien, die eine Chlorquelle sind. Die Meere und Ozeane enthalten Chloranionen aufgrund der gelösten Salze. Da das Leben auf der Erde aus denselben salzigen Gewässern stammt, enthält die innere Flüssigkeit unserer Organismen auch eine Fülle von Chlorionen.
- Chlor ist ein wichtiger Rohmaterial bei der Herstellung von Salzsäure. Die Verwendung in den Haushalten ist von großer Bedeutung, da es der häufigste Bestandteil bakteriziden Reinigungsprodukts ist. Chlorhaltige Präparate zerstören alle bekannten Bakterien. In Form von Radikalen sind Chloratome extrem reaktiv, wodurch sie starke Karzinogene machen.
Unterschied zwischen Brom und Chlor
Definition
Brom: Brom ist ein nichtmetales chemisches Element der VIIA-Gruppe des Periodensystems, das unter normalen Bedingungen eine rotbraune Flüssigkeit mit einem hoch irritierenden Geruch ist.
Chlor: Chlor ist ein nichtmetales chemisches Element der VIIA-Gruppe des Periodensystems, das unter normalen Bedingungen in Form eines grünlich-gelben Gases mit einem hoch irritierenden Geruch ist.
Periodische Zahl
Brom: Brom ist die Nummer 35 in der Periodenzüchtertabelle.
Chlor: Chlor ist die Nummer 17 in der Periodenzüchtertabelle.
Atommasse
Brom: Die Atommasse von Brom beträgt 79.904.
Chlor: Die Atommasse von Chlor beträgt 35.453.
Reaktivität
Brom: Brom ist weniger reaktiv als Chlor. Unter normalen Bedingungen nimmt Brom jedoch an mehreren chemischen Wechselwirkungen teil.
Chlor: Chlor ist ein extrem aktives chemisches Element.
Oxidationszustand
Brom: Oft zeigt Brom in den chemischen Verbindungen einen Oxidationszustand von -1.
Chlor: Chlor kann in allen Oxidationszuständen von -1 bis +7 vorhanden sein, außer +2. Es ist ein starkes Oxidationsmittel und in seinen chemischen Verbindungen am häufigsten von -1 Oxidationszustand.
Vorkommen in der Natur
Brom: In der Natur tritt Brom in Form einer Mischung aus zwei stabilen Isotopen auf. Es ist als Unreinheit in den Chlormineralien Halit (NaCl - Salz), Sylvite (KCL), Carnallit (Kaliummagnium -Hexahydrat) usw. enthalten. Der Gehalt im Meerwasser beträgt ungefähr 1: 660 Chloratome.
Chlor: In der Natur tritt Chlor nur in Form chemischer Verbindungen auf oder dissoziiert in Form von Ionen. Die Mineralien, die eine Chlorquelle sind. Meerwasser enthält Chloranionen aufgrund der gelösten Salze.
Verwenden
Brom: Die Verwendung von Brom umfasst pharmazeutische Präparate, Pestizide, Farbstoffe, Flammschutzmittel, Desinfektion von Pools usw. In der Vergangenheit wurde Kaliumbromid als Beruhigungsmittel und Antikonvulsiva verwendet.
Chlor: Chlor wird als Rohstoff bei der Herstellung von Salzsäure in den Haushalten als häufigsten Bestandteil von bakteriziden Reinigungsprodukten für die Desinfektion von Pools usw. verwendet.
Brom vs. Chlor: Vergleichstabelle
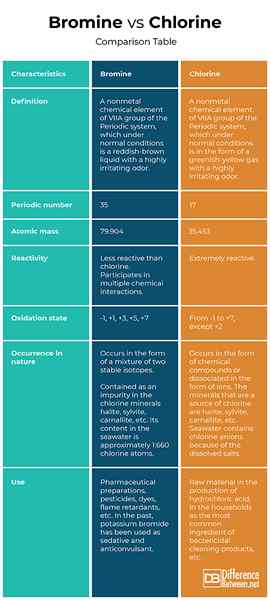
Zusammenfassung von Brom vs. Chlor
- Brom ist ein nichtmetales chemisches Element der VIIA-Gruppe des Periodensystems, das unter normalen Bedingungen eine rotbraune Flüssigkeit mit einem hoch irritierenden Geruch ist.
- Chlor ist ein nichtmetales chemisches Element der VIIA-Gruppe des Periodensystems, das unter normalen Bedingungen in Form eines grünlich-gelben Gases mit einem hoch irritierenden Geruch ist.
- Brom ist die Nummer 35 in der Periodenzüchttabelle und Chlor ist Nummer 17.
- Die Atommasse von Brom beträgt 79.904, die Atommasse von Chlor beträgt 35.453.
- Brom ist weniger reaktiv als Chlor. Unter normalen Bedingungen nimmt Brom jedoch an mehreren chemischen Wechselwirkungen teil.
- Oft zeigt Brom in den chemischen Verbindungen einen Oxidationszustand von -1, aber es kann auch in jedem seltsamen positiven Oxidationszustand sein (+1, +3, +5, +7). Chlor kann in allen Oxidationszuständen von -1 bis +7 vorhanden sein, außer +2.
- In der Natur tritt Brom in Form einer Mischung aus zwei stabilen Isotopen auf. Chlor tritt nur in Form chemischer Verbindungen auf oder dissoziiert in Form von Ionen.
- Die Verwendung von Brom umfasst pharmazeutische Präparate, Pestizide, Farbstoffe, Flammschutzmittel, Desinfektion von Pools usw. In der Vergangenheit wurde Kaliumbromid als Beruhigungsmittel und Antikonvulsiva verwendet. Chlor wird als Rohstoff bei der Herstellung von Salzsäure in den Haushalten als häufigsten Bestandteil von bakteriziden Reinigungsprodukten für die Desinfektion von Pools usw. verwendet.
- « Unterschied zwischen Doug Ford und Donald Trump
- Unterschied zwischen realen Diamanten und gefälschten Diamanten »

